Calorímetro de bomba QualiBC-1600L
Producto principal
Estándares
Calorímetro de bomba QualiBC-1600L
El calorímetro de bomba QualiBC-1600L está diseñado para medir el poder calorífico de combustibles sólidos y líquidos como carbón, coque, petróleo, mezcla cruda de cemento, combustibles de biomasa y materiales de construcción.
- Dimensiones de la unidad principal: 390 × 565 × 485 mm
- Dimensiones del depósito de agua: 220 × 565 × 410 mm
- Peso de la unidad principal: 50 kg
- Peso del depósito de agua: 25 kg

Conformidad con las normas
El calorímetro de bomba QualiBC-1600L cumple con las siguientes normas internacionales:
- ASTM D5865 – Método de ensayo estándar para determinar el poder calorífico bruto del carbón y el coque.
- ASTM D240 – Método de ensayo estándar para determinar el calor de combustión de combustibles líquidos de hidrocarburos utilizando un calorímetro de bomba.
- ASTM D4809 – Método de precisión para determinar el calor de combustión de combustibles líquidos de hidrocarburos mediante calorímetro de bomba.
- ISO 18125 – Biocarburantes sólidos: Determinación del poder calorífico.
- ISO 1928 – Combustibles minerales sólidos: Determinación del poder calorífico bruto mediante el método calorimétrico de bomba y cálculo del poder calorífico neto.
- ISO 9831 – Alimentos para animales, productos animales y excrementos: Determinación del poder calorífico bruto utilizando un calorímetro de bomba.
- ISO 1716 – Ensayos de reacción al fuego de productos: Determinación del calor bruto de combustión (valor calorífico).
Características del calorímetro de bomba QualiBC-1600L
Diseño optimizado y automatización avanzada
- El sistema cuenta con un diseño totalmente automático para las operaciones de llenado y liberación de oxígeno, así como para la elevación de la bomba. Su exclusivo sistema de circulación de agua determina automáticamente el volumen de agua para cada prueba, garantizando precisión y uniformidad.
- La bomba de oxígeno de acero inoxidable de nuevo diseño es fácil de montar y desmontar, mientras que la hélice de alta eficiencia proporciona una agitación superior y una transferencia de calor más rápida. Cada análisis se puede completar en menos de 11 minutos por muestra.
- El innovador mecanismo automático de llenado y liberación de oxígeno mediante presión elimina los bloqueos y proporciona una mayor estabilidad en comparación con los calorímetros automáticos convencionales.

- El sistema está equipado con un depósito de agua termostático semiconductor que proporciona funciones de calefacción y refrigeración. Garantiza un control de temperatura de alta precisión con un menor consumo energético y un nivel de ruido reducido en comparación con los sistemas convencionales basados en compresores.
- Con un alto nivel de automatización, la unidad realiza automáticamente el izado y descenso de bombas, el llenado y liberación de oxígeno, la detección de presión y hermeticidad, el ajuste constante del volumen de agua, el control de temperatura, el lavado de tuberías y el reemplazo de agua.
- El sistema de encendido láser incorporado simplifica el funcionamiento; no requiere la instalación de cables de encendido.
Resultados de pruebas precisos y confiables
- La gran capacidad calorífica del sistema garantiza resultados de medición altamente precisos y consistentes. Admite dos métodos de ignición —alambre de níquel e hilo de algodón—, lo que ofrece flexibilidad para diversos requisitos de prueba.
Diseño fiable, seguro y ecológico
- El sistema presenta un diseño robusto y fiable que garantiza un funcionamiento seguro y respetuoso con el medio ambiente. Su función de autodiagnóstico detecta con precisión las averías para facilitar el mantenimiento. El soporte del crisol, de diseño exclusivo, aporta comodidad y mejora la experiencia del usuario.
Excelente adaptabilidad y estabilidad ambiental
- El sistema proporciona resultados de ensayo precisos, exactos y fiables en diversas condiciones ambientales. Su tecnología isotérmica multipunto de tubo helicoidal crea un entorno interno controlado y estable —que comprende la camisa y la tapa— con una diferencia de temperatura inferior a 0.05 °C. Este diseño minimiza la influencia de factores externos como el flujo de aire y la temperatura ambiente, lo que garantiza resultados de ensayo consistentes y fiables.
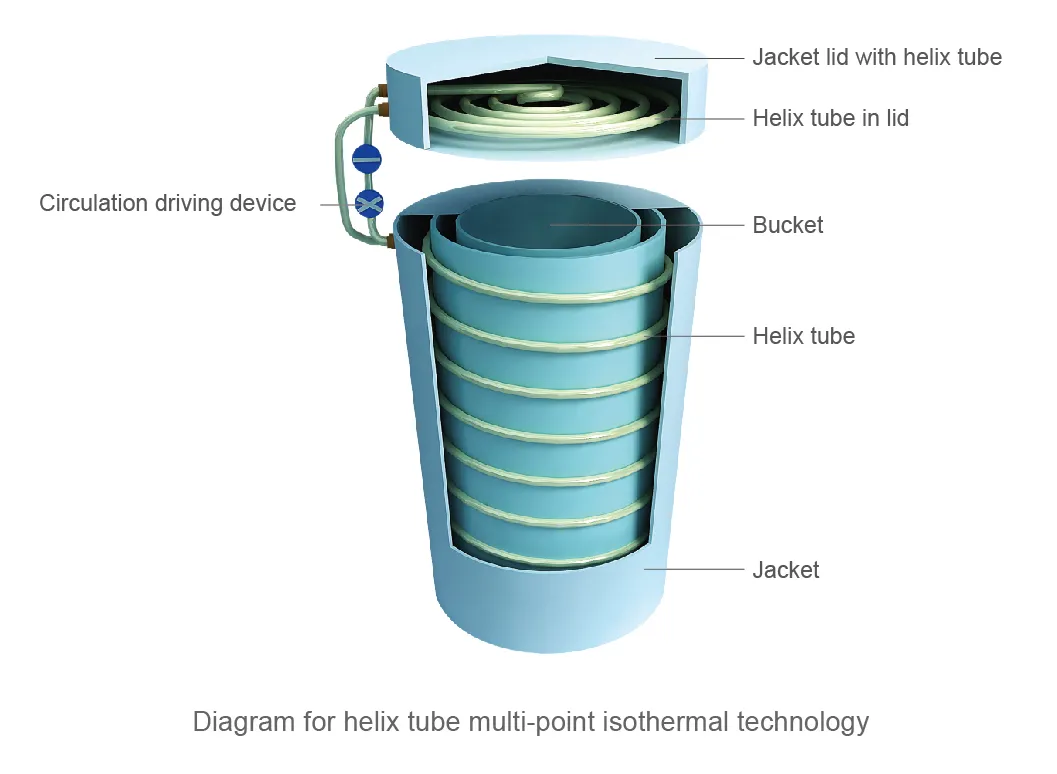
- El sistema cuenta con circuitos de agua independientes para la camisa y el depósito. Tras cada prueba, el agua del depósito retorna automáticamente al tanque, evitando interferencias entre los flujos de entrada y salida del agua del depósito y de la camisa, y manteniendo estable la temperatura del agua de la camisa.
- También incluye detección automática de hermeticidad para evitar fugas de oxígeno que podrían afectar la precisión de las pruebas, junto con monitoreo automático de la presión de oxígeno para garantizar un llenado óptimo, evitando niveles de oxígeno insuficientes y excesivos para obtener resultados confiables.
Especificaciones técnicas del calorímetro de bomba QualiBC-1600L
| Tiempo de análisis | Modo rápido <10 min, Modo estándar <12 min, Modo de precisión <14 min |
|---|---|
| Resolución de temperatura | 0.0001 ℃ |
| Precisión de capacidad calorífica | ≤0.08% |
| Tipo de calorímetro | isoperibólico |
| Método de encendido | láser |
| Estabilidad de la capacidad calorífica | ≤0.20% dentro de 12 meses |
| Conexión de equilibrio | RS232 |
| Requisito de voltaje | 220 V ± 10 %, 50/60 Hz (también disponible en 110 V) |





